Kategorier
Siste innlegg
Nytt medikament mot Alzheimers sykdom
I juni godkjente Det amerikanske mat- og medikamentdirektoratet (FDA) et nytt medikament mot Alzheimers sykdom, aducanumab, som blir markedsført under navnet Aduhelm. En rekke fagfolk mener at medikamentet aldri burde vært godkjent. Her får du bakgrunnen.
Tekst Iver Mysterud
Kort fortalt
I juni godkjente Det amerikanske mat- og medikamentdirektoratet (FDA) et nytt medikament mot Alzheimers sykdom, aducanumab (Aduhelm). En rekke fagfolk mener at det aldri burde vært godkjent. FDA godkjente aducanumab til tross for at dets eget uavhengige rådgivende panel gikk imot. Det finnes ingen dokumentasjon på at medikamentet er til nytte for pasienter med Alzheimers sykdom. Derimot gir det en rekke alvorlige bivirkninger, og prisen for behandling av én pasient er dyr. Godkjenningen har skapt mye debatt i USA, og to komiteer i den amerikanske kongressen gransker både godkjenningsprosessen og den høye prisen. Selv om aducanumab fjerner plakk i hjernen, gir det ikke bedre kognitiv funksjon.
FDA godkjente aducanumab til tross for at ti medlemmer av dets eget uavhengige rådgivende panel stemte mot å godkjenne det, mens én var usikker. Ingen stemte for.1 Noen medlemmer av rådgivningspanelet kalte dette den verste godkjenningen FDA noen sinne har gjort og trakk seg deretter fra panelet. Nettsiden Medscape har gjort en undersøkelse blant nevrologer som kjenner medikamentet, og nesten 90 prosent av dem mente at det ikke burde vært godkjent.2
I de kliniske forsøkene deltok kun pasienter med mild kognitiv svikt. FDA har imidlertid godkjent det for alle med Alzheimers sykdom, som inkluderer alt fra mild til svært alvorlig kognitiv svikt.3
Det finnes ingen dokumentasjon på at medikamentet er til nytte for pasienter med Alzheimers sykdom. Derimot gir det en rekke alvorlige bivirkninger og må gis intravenøst på et legekontor eller sykehus. Prisen for behandling av én pasient i ett år er i USA 56 000 dollar, over 500 000 kroner.2,3 Godkjenningen har skapt mye debatt i USA, og to komiteer i den amerikanske kongressen gransker både godkjenningsprosessen og den høye prisen.1
Som den naturopatiske legen Michael T. Murray fra USA skrev i et nyhetsbrev, ser godkjenningen av aducanumab ut til å være nok et eksempel på at FDA tjener ”Big Pharma” i stedet for pasientene.2 Det har vist seg at FDA har hatt mye tettere samarbeid med produsenten av aducanumab enn det som er vanlig i en godkjenningsprosess.1
Murray har i sin bok The longevity matrix vist hvordan det er mulig å forebygge og til og med reversere Alzheimers sykdom og aldersrelatert hukommelsestap hvis kostholds- og livsstilstiltak settes inn tidlig i sykdomsprosessen.4 Dette har også den amerikanske nevrologen Dale E. Bredesen (f. 1952) vist er mulig.5,6,7,8,9 Hans protokoll ReCODE (Reversing COgnitive DEcline = reversering av kognitiv svikt) er gjentatte ganger omtalt i Helsemagasinet (se ramme).
Tidligere i Helsemagasinet om Dale E. Bredesen og hans protokoll
Mysterud I. Helhetlig terapi mot kognitiv svekkelse og Alzheimers sykdom. VOF 2017; 8 (7): 22–7.
Mysterud I. Suveren bok om Alzheimers sykdom. VOF 2017; 8 (8): 60–3.
Mysterud I. Klar for å motvirke utvikling av demens. VOF 2018; 9 (7): 60–2.
Mysterud I. Fornyet håp om bedring ved Alzheimers sykdom. VOF 2019; 10 (1): 14–6.
Mysterud I. Vellykket test av bred alzheimerprotokoll. VOF 2021; 12 (4): 36–7.
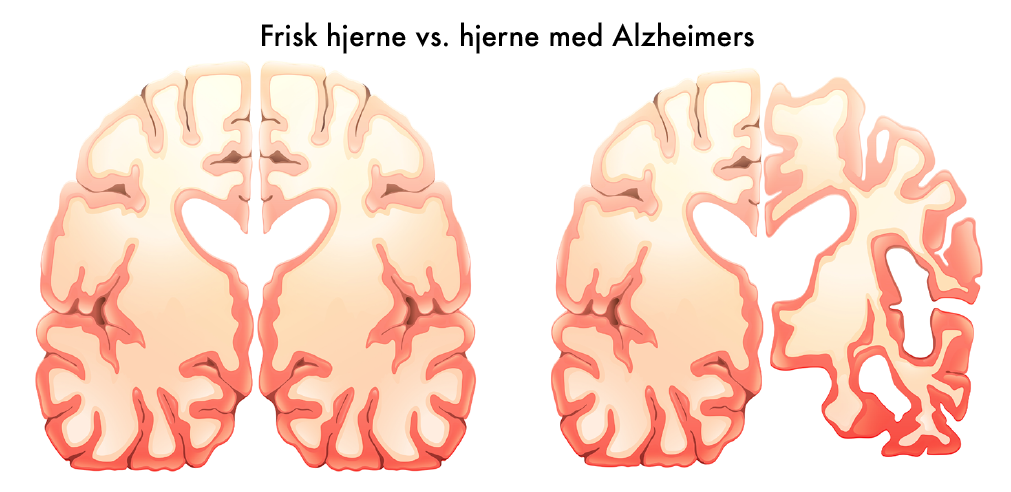
Liten vitenskapelig støtte
Bredesen har også uttalt seg kritisk til aducanumab, blant annet på Facebook. Et kjennetegn ved Alzheimers sykdom er at det avleires plakk mellom nervecellene. Hvis disse avleiringene fortsetter, skader det hjernen. Derfor har en rekke forskere testet effekten av å fjerne plakket med ulike typer medikamenter, slik som solanezumab og bapineuzumab, og nå aducanumab. Slike medikamenter har imidlertid ikke bedret de kognitive prosessene hos de sykdomsrammede. Ifølge Bredesen var aducanumab til og med verre enn placebo i ett forsøk. I et annet forsøk verken bedret eller stabiliserte medikamentet de kognitive prosessene, selv om det forsinket en videre nedgang i deltakernes kognitive evne med om lag en femdel.10
Ifølge Bredesen har forskning ettertrykkelig vist at de nevnte medikamentene ikke bedrer kognitive prosesser, til tross for at de fjerner plakk. FDA konkluderte motsatt: Fordi medikamentet fjernet plakk, var det rimelig å forvente at det bedret kognitive prosesser, noe som altså er motsatt av hva studiene viste.10
Bredesens oppfordring til pasienter er klar: Ikke vent til man opplever en nedgang i kognitive prosesser for så å ta et medikament som kun reduserer tempoet i prosessen litt. Det er fullt mulig å forebygge og reversere kognitiv svikt med skreddersydde protokoller som ReCODE, til en brøkdel av kostnaden til ineffektive medikamenter som aducanumab.10
Aducanumab i Norge
Dette medikamentet er i øyeblikket under vurdering hos Det europeiske legemiddelverket (EMA). Hvis innstillingen til EMA er positiv til aducanumab, vil EU-kommisjonen normalt fatte et vedtak om markedsføringstillatelse som er gyldig i alle medlemslandene i EU. EØS-landene Norge og Island må utstede egne nasjonale markedsføringstillatelser innen 30 dager etter at kommisjonen har fattet sitt vedtak. Hvorvidt det nye medikamentet blir tatt i bruk i det enkelte land, avhenger derimot av hva legemiddelfirmaet selv ønsker og om myndighetene i landet innvilger refusjon eller ikke.11
Kilder:
1 Belluck P, Kaplan S, Robbins R. How an unproven Alzheimer’s drug got approved. The New York Times 2021; 19. juli. https://www.nytimes.com/2021/07/19/health/alzheimers-drug-aduhelm-fda.html
2 Murray M. The FDA does it again! Nyhets-e-post 11.7.2021.
3 Robbins R, Belluck P. Alzheimer’s drug is bonanza for Biogen, most likely at taxpayer expense. The New York Times 2021; 8. juli. https://www.nytimes.com/2021/06/08/business/aducanumab-alzheimers-cost.html
4 Murray MT. The longevity matrix: How to live better, stronger, and longer. Morgan James Publishing, 2021.
5 Bredesen D. The end of Alzheimer’s: The first programme to prevent and reverse the cognitive decline of dementia. London: Vermillion, 2017. Norsk versjon: Stopp Alzheimer: Hvordan forebygge og reversere Alzheimers. Oslo: Cappelen Damm, 2020.
6 Bredesen DE. Reversal of cognitive decline: a novel therapeutic program. Aging 2014; 6: 707–17. https://www.ncbi.nlm.nih.gov/pubmed/25324467
7 Bredesen DE, Amos EC, Canick J mfl. Reversal of cognitive decline in Alzheimer’s disease. Aging 2016; 8: 1250–8. https://www.ncbi.nlm.nih.gov/pubmed/27294343
8 Bredesen DE, Sharlin K, Jenkins D mfl. Reversal of cognitive decline: 100 patients. Journal of Alzheimer’s Disease & Parkinsonism 2018; 8: 450. https://www.omicsonline.org/open-access/reversal-of-cognitive-decline-100-patients-2161-0460-1000450.pdf
9 Toups K, Hathaway A, Gordon D mfl. Precision medicine approach to Alzheimer’s disease: Successful proof-of-concept trial. medRxiv 11.5.2021. https://www.medrxiv.org/content/10.1101/2021.05.10.21256982v1.full
10 E-post fra Dale E. Bredesen til IM 9.6.2021.
11 E-post fra rådgiver Nils Gunnar Løvsletten i Statens legemiddelverk 14.6.2021.