Kategorier
Siste innlegg
Sannheten om kreft – standardteorien utfordres
I Helsemagasinet nr. 4/2018 presenterte vi første del av en gjennomgang av boka til Travis Christoffersen, Tripping over the truth. Der beskrev vi hvorfor forfatteren ble interessert i kreftforskning og hvordan han kom fram til at nobelprisvinner i medisin eller fysiologi Otto H. Warburg trolig hadde rett om årsakene til kreft, til tross for at han ble glemt. Forfatteren viste til nyere arbeid av ”andregenerasjons pionerer” og nøstet videre for å undersøke hvorvidt nyere forskning kunne bekreft Warburgs originale kreftforskning.
Tekst Dag Viljen Poleszynski Foto Shutterstock
Kort fortalt
- Ifølge Travis Christoffersens er dagens forklaringsmodell for kreft gal.
- Den rådende oppfatningen er at kreft skyldes skader på cellekjernens DNA, og at dette fører til ukontrollert vekst.
- Forskning utført helt fra 1920-tallet viser at kreft er en stoffskiftesykdom som ikke forårsakes av skader på DNA
i cellekjernen, men av skader på mitokondriene. - Skadde mitokondrier sender ”nødsignaler” til cellekjernens DNA. Dette fører til at DNA aktiverer en rekke onkogener (”kreftgener”), som igjen aktiverer uhemmet celledeling.
- Kreft er en evolusjonær tilpasning som stimulerer deling og vekst ved skader på stoffskiftet.
- Antallet mutasjoner på DNA i samme kreft og ulike krefttyper varierer tilfeldig.
- Christoffersen dokumenterer at ledende forskere nå innrømmer at ”standardmodellen” kan være gal og diskuterer hvilke følger dette kan komme til å få for framtidens kreftbehandling.
Christoffersen beskriver levende hvordan ledende kreftforskere arbeidet videre for å finne de underliggende årsakene til kreft. Historien fortelles springende, og vi vil trekke fram noen hovedpunkter.
En viktig milepæl i kreftforskningens historie skjedde i 1971 da president Richard Milhous Nixon (1913–1994) i en tale til Kongressen erklærte ”krig mot kreft” (s. 60). Dette ble fulgt opp med massive bevilgninger for å forene kreftene blant annet for å finne effektive kombinasjoner av cellegifter som kunne hemme celledeling. Med USAs Nasjonale helseinstitutt (NHI) i spissen utviklet USAs Nasjonale kreftinstitutt seg til en screening-fabrikk med et program som brukte tre millioner mus i året for å gjennomgå 40 000 cellegifter. Nye, lovende giftstoffer gjorde at budsjettet for kliniske forsøk este fra $9 millioner i 1972 til $119 i 1980. En rekke økonomiske interesser samarbeidet med forskere og statlige institusjoner om det som siden slutten av 1960-tallet hadde vært den enerådende teorien for kreft, at det skyldes mutasjoner i DNA.
Forskere fant ut at en kombinasjon av cellegifter drastisk bedret helbredelse av testikkelkreft, fra 10 til 85 prosent (s. 62). Imidlertid var ikke suksessraten særlig stor: i 1985 fikk en million mennesker en kreftdiagnose, og kombinasjonen av cellegifter, stråleterapi og operasjoner hadde bare reddet fire prosent flere siden 1972. Dessuten viste noen av cellegiftene seg å ha alvorlige virkninger på lang sikt: de førte til drastisk økt risiko for hjerteinfarkt og slag, og barn som fikk en ”vellykket” behandling mot Hodgkins sykdom, hadde 18 ganger økt risiko for å utvikle ondartede sekundærsvulster (s. 65). Jenter som var behandlet, kunne forvente 35 prosent sannsynlighet for å utvikle brystkreft innen fylte 40 år – en økt risiko på 75 ganger mer enn normalt.
Etter at Warburg døde i 1970, skrev verdens mest kjent kreftforsker, Sidney Weinhouse1 (1909–2001), i 1976 en artikkel med knusende kritikk av hans arbeider:2 ”Hele ideen om at kreft initieres eller overlever grunnet ´feil´ celleånding og høy glykolyse virker for enkelt til å kunne tas på alvor” (s. 67). DNA ble ansett å inneholde løsningen på ikke bare kreft, men på en rekke andre sykdommer.
På 1980-tallet ble det utviklet nye teknikker for å avdekke gener, og i 1990 ble det store, humane genomprosjektet (HGP) lansert (s. 127). I løpet av de neste 15 åra skulle forskere sekvensere (bestemme rekkefølgen på) alle de tre milliardene baseparene i menneskets DNA. Målet var å lage et kart over sammenhengen mellom genkombinasjoner som viser sykdomstilbøyelighet og andre egenskaper. Etter en del klabb og babb ble prosjektet ledet av genetikeren Francis Seller Collins3 (f. 1950), president og sjefsforsker i bioteknologiselskapet Celera Genomics. HGP kostet skattebetalerne $3 milliarder, inkludert $500 millioner for å sekvensere alle baseparene.
Prosjektet ble fullført i 2003, to år før planlagt, og i 2005 annonserte USAs Nasjonale helseinstitutt (NIH) et storstilet statlig program kalt The Cancer Genome Atlas (TCGA) med den kjente medisinske forskeren Bert Vogelstein (f. 1949) som leder (s. 130). Han var på 1990-tallet en av de sterkeste talsmennene for forestillingen om kreft som genetisk sykdom, og høsten 2006 startet arbeidet med å avdekke ”fingeravtrykk” i form av mutasjoner i ulike typer kreft, først i tykktarmen (s. 131).
Etter hvert som data fra kreftatlaset ble analysert, gjorde forskerne overraskende nok ingen konsistente mønstre som karakteriserte ulike typer kreft! Dessuten fant de bemerkelsesverdig få nye onkogener (kreftgener), og nye analyser av bryst- og tykktarmskreft viste ingen skrittvise endringer i DNA i samme krefttype (s. 132). Mutasjonsmønsteret i ulike celler i hver svulst var høyst heterogent, noe som sjokkerte alle involverte forskere. De fant heller ingen enkeltmutasjon som kunne forklare hvorfor kreften startet, ei heller noen kombinasjoner av mutasjoner som viste dette (s. 133).
I 2008 sekvenserte forskerne genene til 24 individers bukspyttkjertelkreft, uten nye funn som kunne bekrefte standardteorien (s. 134). Slik fortsatte det fram mot 2013, da mer enn 21 000 gener fra 100 brystkreftsvulster var analysert, og resultatene varierte helt tilfeldig! Det viste seg at det heller ikke fantes et mønster som kunne forklare forskjeller mellom ulike krefttyper (s. 137).
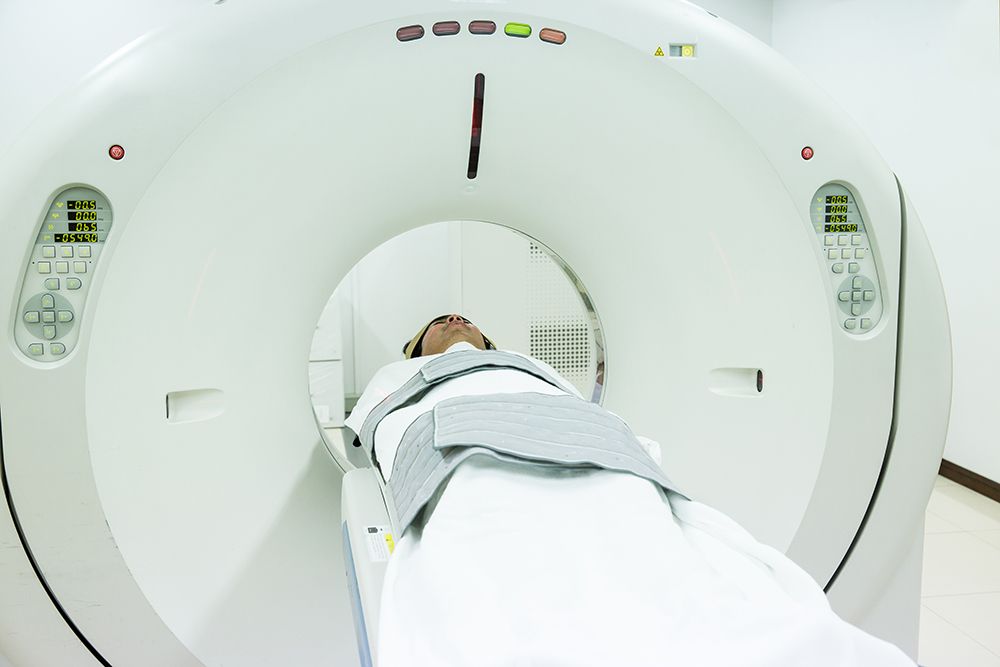
[gdlr_box_icon icon=»none» title=»PET-skanning»]
Identifisering av kreftceller ved hjelp av ansamling av glukose ble svært nøyaktig etter oppdagelsen av en billeddiagnostisk teknikk kalt posisjonsemisjonsto-mografi10 (PET) i 1970. Ved å injisere glukose radio-merket med fluor18 (F-deoksiglukose) i blodet viser PET akkurat hvor kreftceller befinner seg fordi de tiltrekker mye mer glukose enn friske celler (s. 80), og dermed lyser ansamlingen av radiomerket glukose opp på en skjerm.[/gdlr_box_icon]
Delvis innrømmelse
Forskerne lette desperat etter forklaringer etter at det ble klart at den spontane mutasjonsraten som DNA utsettes for, ikke på noen måte korrelerte med den kjente forekomsten av kreft (s. 137). Vogelstein lanserte i 2013 noen originale forslag for å ”redde” den eksisterende teorien, basert på den nye forskningen (ad hoc-forslag):4 Blant annet skyldte forskerne på at gensekvensering var beheftet med falsk-negative resultater på 15–37 prosent, noe de forsøkte å forklare med forekomsten av ”svart materie”, hvilket de ikke fant en rasjonell forklaring på.
Til tross for at PET-skanning (se ramme) hadde bekreftet kreftcellenes appetitt på glukose, slik Warburg og Pedersen hadde vist, ble dette oversett i iveren over å finne DNA-skader (mutasjoner) som kunne føre til kreft. Biologen og kreftforskeren Robert Allan Weinberg5 (f. 1942) var trolig den som mest effektivt fant nye onkogener utover 1980-tallet. Hans forskning befestet forestillingen om at kreft var en genetisk sykdom, en oppfatning som fortsatt dominerer blant kreftforskere, selv om enkelte er i tvil om årsaken.
Blant dem som har vist en viss vilje til å modifisere standardteorien, er Weinberg og kolleger, som i 2000 publiserte en artikkel som beskrev seks kjennetegn ved kreft.6 Da Pedersen i mars 2009 foreleste på et seminar i regi av USAs Nasjonale helseinstitutt (s. 148), påpekte han at Weinberg i artikkelen og en bok om kreft hadde utelatt Warburg-effekten, som nettopp kjennetegner hver eneste krefttype. Etter denne kritikken reviderte Weinberg oppfatning og publiserte en ny artikkel der han la til to nye kjennetegn i ferd med å bli anerkjent, hvorav ett inkluderte at kreftceller ”reprogrammerer energistoffskiftet” – med andre ord Warburg-effekten, som han omtaler i artikkelen, men som han likevel ikke anerkjente.7 Han nevnte ikke mitokondrienes rolle, men hevdet at årsaken lå i cellekjernen og at reprogrammeringen av stoffskiftet skyldes onkogener.
Innrømmelsen av at kreft var en stoffskiftesykdom, skulle først komme
fra tidligere nobelprisvinner James Dewey Watson (f. 1928), som i en artikkel i New York Times i 20098 foreslo å skifte fokus fra genetikk til kreftcellenes stoffskifte (s. 152). Han viste til at Warburg i 1924 fant at alle kreftceller danner store mengder melkesyre og oppfordret til ”modige, nye forsøk på å finne ut om medikamenter som spesifikt hemmer nøkkelenzymer involvert i nedbryting av glukose, motvirker kreft”.
Watson hevdet imidlertid feilaktig at betydningen av Warburgs arbeider først var oppdaget et år tidligere; Pedersen hadde allerede brukt over 30 år på å beskrive i detalj hvorfor og hvordan Warburg-effekten fungerte. I en artikkel fra 20139 skrev Watson at 3-brompyruvat var en kraftig hemmer av heksokinase og oksidativ fosforylering. Han la til at 3BP ”dreper farlige leverceller mer enn 10 ganger raskere enn normale leverceller og har evne til å helbrede, i det minste i rotter, en ellers høyst uhelbredelig kreft”.
Watson uttrykte sterk pessimisme når det gjaldt muligheten til å helbrede kreft med spredning: ”helbredelse [av kreft] virker nå for mange erfarne forskere å være et enda mer utfordrende mål enn da ”krigen mot kreft” ble lansert av president Nixon i desember 1971”.
Mitokondrienes nøkkelrolle
Bokas kapittel 6 omhandler en detaljert beskrivelse av mitokondrienes viktige rolle i kroppens energistoffskifte, inkludert forklaringen på hvordan kreftceller vokser og deler seg ved hjelp av økt glykolyse fordi mitokondriene er skadd. Christoffersen gjentar viktige gjennombrudd av Pedersen og andre, som viste at mitokondrier kan skades både av kjemiske giftstoffer, radioaktiv stråling og virus (s. 166–7), samtidig som det oppstår skade på DNA.
Forfatteren trekker fram de viktige arbeidene til Thomas N. Seyfried (f. 1946), som tidlig forsto at mutasjoner av DNA hadde lite å gjøre med årsaken til kreft. Etter at Seyfried fikk høre om Otto Warburg, jobbet han intenst de neste ti åra før han summerte resultatene av sin forskning i en veldokumentert bok om kreft som en metabolsk sykdom,11 som vi omtalte utførlig i Helsemagasinet i 2015.12 I samme utgave gjennomgikk vi Warburgs forskning og Seyfrieds forskning på kroniske lidelser som epilepsi, degenerative lipidlagringssykdommer i hjernen og kreft. Seyfrieds terapeutiske arsenal inkluderer kalorirestriksjon, faste og ketogen diett.13
Etter grundige studier av sammenhengen mellom kreftcellers ødelagte stoffskifte og ukontrollerte vekst foreslår Seyfried at dette utløser et epigenetisk signal fra mitokondriene til cellekjernens DNA (s. 173). Dette signalet endrer genuttrykket til en rekke onkogener som fører til kreft. Det betyr at de genetiske skadene på DNA som man finner ved kreft, er en følge av nødsignaler fra cellene, ikke en årsak. Han kan dermed ha funnet det siste leddet som mangler i forklaringen på hvorfor og hvordan kreft oppstår.
Dette forklarer Christoffersen i detalj med utgangspunkt i Seyfrieds bok fra 2012. Allerede da var det foretatt en rekke eksperimenter som understøttet en slik forklaring. Genene som responderte på mitokondriell stress, kalles Myc, Tor, Ras, NfkB og CHOP, og styrer en rekke funksjoner som celledeling og nydanning av blodårer (angiogenese). I tillegg til å stimulere en massiv økning i enzymer som øker ATP-produksjonen i glykolysen, gir blant annet Myc bivirkninger som ukontrollert celledeling!
Ifølge Seyfried skjer mutasjonene som postuleres å utgjøre virkningen i standardmodellen for kreft, nedstrøms for den virkelige årsaken: ødelagte mitokondrier. Mutasjonene er en bivirkning, et epifenomen. Mutasjoner som observeres i DNA, er ifølge Seyfried virkninger snarere enn årsak til kreftutvikling (s. 175). Endringene i DNA har i mange tiår ført kreftforskere på en nytteløs leting og dermed forhindret effektive terapier.
Kreftsvulster kan fjernes kirurgisk, bestråles eller utsettes for cellegifter. Slik terapi er ikke årsaksrettet, men har gitt grunnlag for en gigantindustri som arbeider ”nedstrøms” – etter at problemet har oppstått. En bedre løsning er å forhindre at kreft oppstår, noe som ifølge Warburg krever at cellene får tilført nok oksygen og at mitokondriene ikke skades av miljøgifter eller virus. Veksten av kreft kan hemmes ved å ”strupe” cellene for glukose, noe stadig flere kreftforskere har oppdaget.
Warburg: stadig flere tilhengere
I resten av boka forklarer Christoffersen levende framveksten av forskning av en rekke forskere som i likhet med Seyfried anbefaler blant annet faste og ketogen kost mot kreft og en rekke nevrologiske sykdommer. Linda Nebeling, PhD, dokumenterte allerede i 1995 nytten av ketogen kost mot kreft (s. 196), og blant andre forskere nevner han veteranene Richard Veech og Walter Longo, som begge har publisert tallrike vitenskapelige artikler om temaet.
Etter å ha lest Christoffersens bok er vår konklusjon at etablerte kreftforskere har lett i feil retning i årtier, noe som gjenspeiles i relativt små bedringer når det gjelder overlevelse av kreft. Den unisone troen på ”Standardmodellen” har vært et gedigent feilspor: Modellen forklarer ikke hvordan kreft oppstår og gir derfor heller ikke grunnlag for å finne rasjonelle, virksomme terapier mot kreft.
Vi anbefaler Tripping over the truth på det varmeste og håper at også norske kreftleger vil ta inn over seg forfatterens budskap.
Forfatter: Travis Christoffersen
Tittel: Tripping over the truth. How the metabolic
theory of cancer is overturning one of medicine´s
most entrenched paradigms.
Utgiver: Chelsea Green Publishing (Vermont/USA, London/UK (2. utgave).
Utgivelsesår: 1. utgave 2014 (272 sider, heftet),
2. utgave 2017 (258 sider innbundet;
ISBN 1098 7654 321
Pris: Fra £ 4,92 (heftet) fra amazon.co.uk;
$24,95 fra chelseagreen.com
Kilder:
1. Hanson GM, Hanson RW. Sidney Weinhouse 1909–2001. A biographical memoir. National Academy of Sciences, Washington, D.C. 2009. http://www.nasonline.org/publications/biographical-memoirs/memoir-pdfs/weinhouse-sidney.pdf (14.5.2018).
2. Weinhouse S. The Warburg hypothesis fifty years later. Zeitschrift für Krebsforschung und klinische Onkologie 1976; 87: 115–26. https://www.ncbi.nlm.nih.gov/pubmed/136820
3. Shampo MA, Kyle RA. Francis S. Collins – Human Genome Project. Mayo Clinic Proceedings 2010; 85: e-66–7. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2931629/
4. Vogelstein B, Papadopoulos N, Velculescu VE mfl. Cancer genome landscapes. Science 2013; 339: 1546–58. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3749880/
5. https://en.wikipedia.org/wiki/Robert_Weinberg (3.5.2018).
6. Hanahan D, Weinberg RA. The hallmarks of cancer. Cell 2000; 100: 57–70. https://www.ncbi.nlm.nih.gov/pubmed/21376230
7. Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation. Cell 2011; 144: 646–74. https://www.ncbi.nlm.nih.gov/pubmed/21376230
8. Watson JD. To fight cancer, know the enemy. The New York Times 5.8.2009. https://www.nytimes.com/2009/08/06/opinion/06watson.html
9. Watson J. Oxidants, antioxidants and the current incurability of metastatic cancers. Open Biology
2013; 3: 120144. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3603456/
10. https://no.wikipedia.org/wiki/Positronemisjonstomografi (3.5.2018).
11. Seyfried TN. Cancer as a metabolic disease. Hoboken, NJ: John Wiley & Sons, Inc.
12. Poleszynski DV. En epokegjørende bok. VOF 2015; 6 (5): 42–7.
13. Poleszynski DV. Er kreft en stoffskiftesykdom? VOF 2015; 6 (5): 38–41.